ANVISA REJEITA NOVOS MEDICAMENTOS PARA DIABETES E OBESIDADE NO BRASIL
Decisão barra entrada imediata de alternativas mais baratas e mantém mercado concentrado
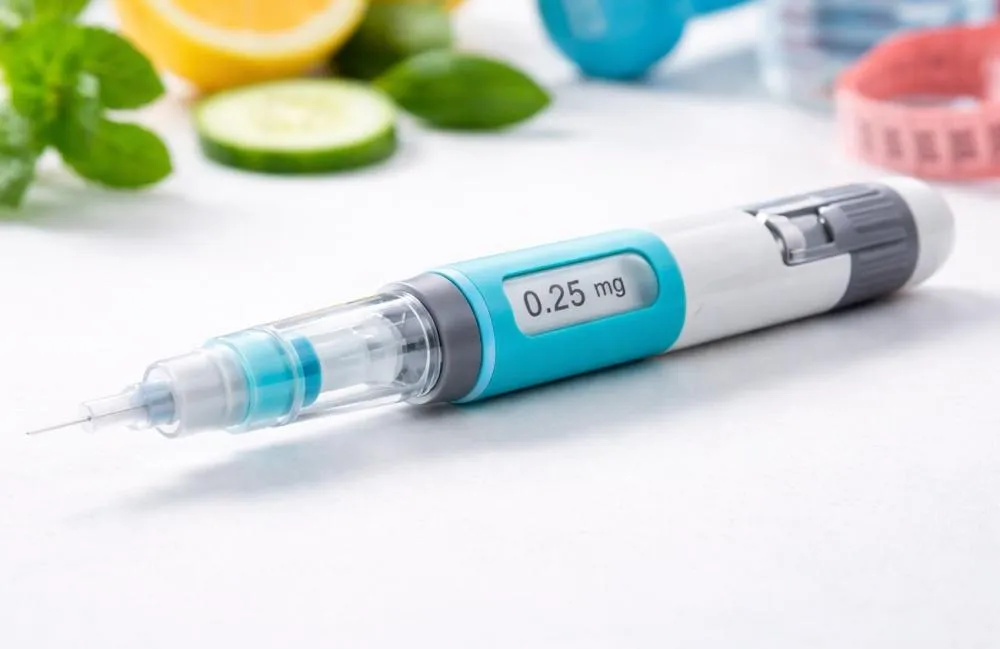
A Agência Nacional de Vigilância Sanitária rejeitou pedidos de registro de novos medicamentos à base de semaglutida e liraglutida, substâncias amplamente utilizadas no tratamento do diabetes tipo 2 e da obesidade. A decisão foi publicada no Diário Oficial da União nesta segunda-feira (13) e impede, por ora, a comercialização de três produtos no país.Foram indeferidos dois medicamentos à base de liraglutida, da farmacêutica Cipla, e um de semaglutida, da Dr. Reddy’s. Os pedidos estavam sendo analisados por meio do chamado “desenvolvimento abreviado”, modalidade que permite às empresas utilizarem dados já existentes sobre as substâncias para tentar acelerar a aprovação. Apesar disso, a Anvisa reforça que não há flexibilização nos critérios de segurança, eficácia e qualidade. As farmacêuticas precisam apresentar dados próprios consistentes, e, na ausência de comprovação suficiente, os pedidos são negados, como ocorreu neste caso.
Com a decisão, a entrada de novos concorrentes no mercado brasileiro fica adiada, mantendo a concentração nas marcas já disponíveis e contribuindo para a continuidade da oferta restrita e dos altos preços desses tratamentos, que vêm registrando forte demanda.O cenário ocorre em um momento estratégico para o setor farmacêutico, após o fim da patente da semaglutida — substância presente em medicamentos conhecidos como Ozempic e Wegovy — que abriu espaço para novas empresas tentarem ingressar no mercado após cerca de duas décadas de exclusividade.
No Brasil, ao menos 17 pedidos de registro já foram apresentados à Anvisa, mas nenhum foi aprovado até o momento. A complexidade da semaglutida, considerada uma molécula de difícil desenvolvimento, exige um rigor ainda maior nas análises, o que prolonga o processo regulatório.Atualmente, alguns desses pedidos mais avançados seguem em fase de exigências técnicas, etapa em que a agência solicita informações adicionais antes de uma decisão final. A expectativa do setor é que as primeiras versões alternativas possam ser aprovadas ao longo de 2026, dependendo da qualidade dos dados apresentados.
A possível entrada desses novos medicamentos é vista como fundamental para ampliar a oferta e, no médio prazo, reduzir os preços — cenário que ainda não se concretizou no país.
 PONTE RECONSTRUÍDA RECONSTRUÇÃO DA PONTE DA CAFELÂNDIA AVANÇA E ATENDE ANTIGA DEMANDA DE MORADORES
PONTE RECONSTRUÍDA RECONSTRUÇÃO DA PONTE DA CAFELÂNDIA AVANÇA E ATENDE ANTIGA DEMANDA DE MORADORES  MEMORIAL DA COVID BRASIL CRIA MEMORIAL DA PANDEMIA EM HOMENAGEM ÀS MAIS DE 700 MIL VÍTIMAS DA COVID-19
MEMORIAL DA COVID BRASIL CRIA MEMORIAL DA PANDEMIA EM HOMENAGEM ÀS MAIS DE 700 MIL VÍTIMAS DA COVID-19  DIREITO A ISENÇÃO PACIENTES COM CÂNCER TÊM DIREITO À ISENÇÃO DE IMPOSTO DE RENDA E BENEFÍCIOS SOCIAIS
DIREITO A ISENÇÃO PACIENTES COM CÂNCER TÊM DIREITO À ISENÇÃO DE IMPOSTO DE RENDA E BENEFÍCIOS SOCIAIS  A COVID SEGUE NOVA SUBVARIANTE DA COVID-19, ‘CICADA’ TEM 75 MUTAÇÕES E JÁ CIRCULA EM 23 PAÍSES; VEJA O QUE SE SABE
A COVID SEGUE NOVA SUBVARIANTE DA COVID-19, ‘CICADA’ TEM 75 MUTAÇÕES E JÁ CIRCULA EM 23 PAÍSES; VEJA O QUE SE SABE  VISITA ILUSTRE GOVERNADOR DE MINAS GERAIS VISITA BISPO DE LEOPOLDINA, DOM EDSON ORIOLO
VISITA ILUSTRE GOVERNADOR DE MINAS GERAIS VISITA BISPO DE LEOPOLDINA, DOM EDSON ORIOLO  PRAZO PRORROGADO GOVERNO PRORROGA PRAZO PARA CONTESTAÇÃO DE DESCONTOS INDEVIDOS NO INSS ATÉ 20 DE JUNHO
PRAZO PRORROGADO GOVERNO PRORROGA PRAZO PARA CONTESTAÇÃO DE DESCONTOS INDEVIDOS NO INSS ATÉ 20 DE JUNHO Mín. 18° Máx. 25°
Mín. 18° Máx. 26°
Parcialmente nubladoMín. 16° Máx. 26°
Tempo limpo







